标新生物再次联合发表文章,设计开发新型分子胶
发布日期:2022-12-21 文章来源:标新生物
近日,标新生物、上海科技大学以及南华大学联合在国际学术期刊《European Journal of Medicinal Chemistry》上发表题为“Design, synthesis and biological evaluation of novel quinazolinone derivatives as CRBN E3 ligase modulators”的研究论文。该文章设计了一系列结构新颖的CRBN调节剂,表现出强劲的蛋白降解活性,可为多发性骨髓瘤、弥漫大 B 细胞淋巴瘤的治疗提供新型候选化合物。CRBN调节剂,也称为免疫调节药物(IMiDs),通过诱导Cereblon(CRBN)降解包括转录因子在内的多种底物而表现出良好的药理活性,已成为药物开发的一个重要方向。沙利度胺(Thalidomide)、来那度胺(Lenalidomide)、泊马度胺(Pomalidomide)等调节剂诱导CRBN粘附IKZF1、IKZF3等新底物,进而导致这些底物被泛素化降解,从而延缓多发性骨髓瘤等疾病的进一步发展(图1)。相较于当前热门的PROTAC而言,CRBN调节剂具有分子量小、可降解 “unligandable”蛋白的优势,因此受到越来越多的关注和研究。
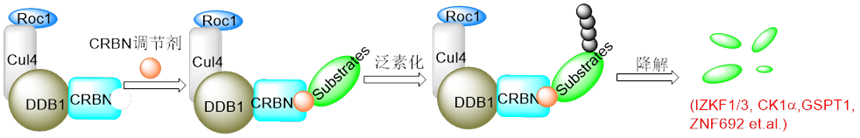
图1 CRBN调节剂的降解机制
CC-122是一种喹唑啉酮类似物,在降解IKZF1/3方面比来那度胺有更强的活性,但对SALL4(spallike transcription factor 4,一种导致沙利度胺致畸的关键蛋白)的作用显著减弱,因而在B细胞恶性肿瘤的治疗中显示出更大的治疗窗口。尽管CC-122降解活性强,药代动力学性质优良,但目前鲜有研究对CC-122进行优化。本论文通过在CC-122喹唑啉酮上引入各类取代基,试图探明CC-122构效关系并获得降解活性更优的衍生物(图2)。经过抗增殖活性研究、降解活性评价和体内外药物代谢动力学研究,发现最佳化合物 SIAIS355035(化合物14)表现出比CC-122更好的降解活性和抗增殖活性,特别是抗弥漫大B细胞淋巴瘤细胞系增殖具有显著优势。此外,化合物SIAIS355035的口服生物利用度等PK性质也显示出优良的特性(图3)。这些结果表明了CC-122具有进一步优化的空间,初步证明化合物SIAIS355035可作为一种理想的新型CRBN调节剂被进一步研究。
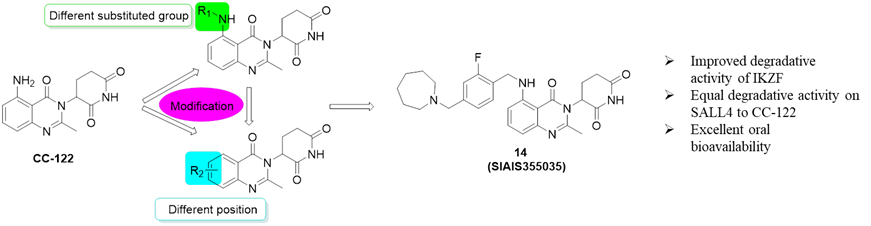
图2 基于CC-122的衍生化修饰
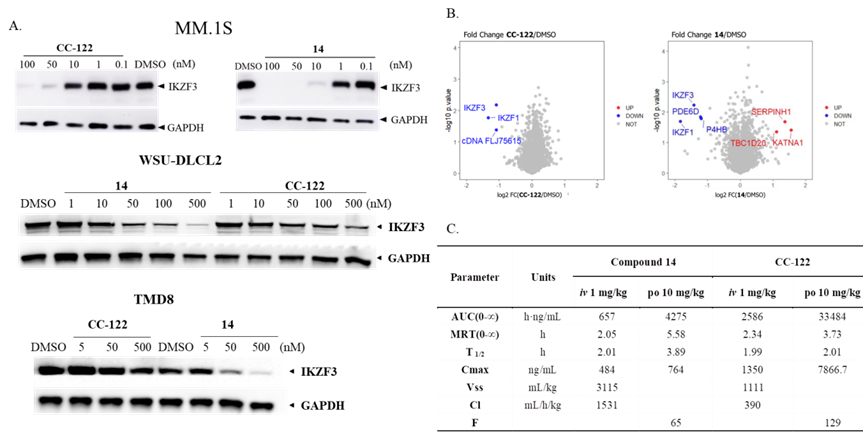
图3 化合物SIAIS355035在多种癌细胞中展现出良好的降解活性,并具备优良药代动性质
发表文章链接:https://doi.org/10.1016/j.ejmech.2022.115016
致谢:此项研究得到了国家重点研发计划2022YFC3401500等资金支持。
该文章是标新生物成立以来与学术机构合作在线发表的第六篇通讯单位文章,此篇学术论文的发表体现了标新生物基于对构效关系的深刻洞察进行理性设计的设计理念,为构建丰富多样的分子胶降解剂和GLUETAC降解剂化合物库奠定了坚实的基础。