标新生物和上海科技大学科研团队联合发表文章,首次报道了在肿瘤中实现ROS诱导的PROTAC前体药物释放
发布日期:2022-08-17 文章来源:标新生物
近日,标新生物和上海科技大学科研团队在国际知名期刊《Chemical Communications》在线发表了题为“Reactive oxygen species-responsive Pre-PROTAC for tumor specific protein degradation”的文章,这是关于ROS诱导PROTAC前体特异性释放的开篇之作,这一开创性工作标志着PROTAC的开发将逐步走向高度组织特异性和肿瘤特异性,为针对广泛表达的致病蛋白开发PROTAC开辟了方向。
ROS(Reactive oxygen species)是活性氧物质的统称,如超氧化物、过氧化氢、羟基自由基等,在细胞中扮演着非常重要的角色,对生理和信号通路调节起到重要的作用。在正常的细胞中,ROS的含量较低,但是在肿瘤微环境中,ROS含量远高于正常组织。ROS可以推进肿瘤的发生和发展,包括癌症信号的激活、抑癌基因的缺失、调控肿瘤转移等等。研究称,肿瘤细胞中的ROS含量可以达到100 μM,远远高于正常的细胞。
科研团队首次利用ROS实现化学控制的PROTAC的活性释放,且只在ROS含量高的肿瘤细胞中特异释放,而对正常细胞没有释放降解活性。如图1所示。
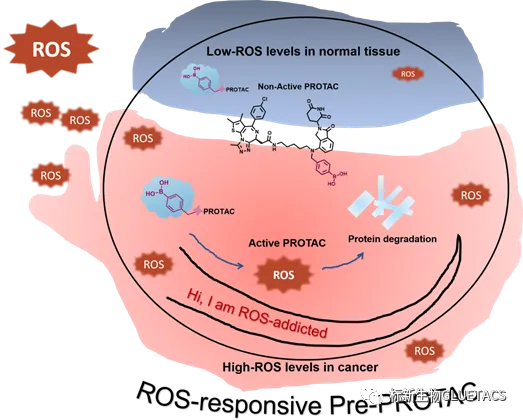
图1
首先,团队通过设计和筛选不同结构的ROS诱导的Pre-PROTAC,通过无细胞实验选择合理的连接位点和释放条件,得到Pre-PROTAC(7)作为合理的ROS诱导型的蛋白降解剂。在双氧水的条件下,Pre-PROTAC(7)可释放出有活性的蛋白降解剂。如图2所示。
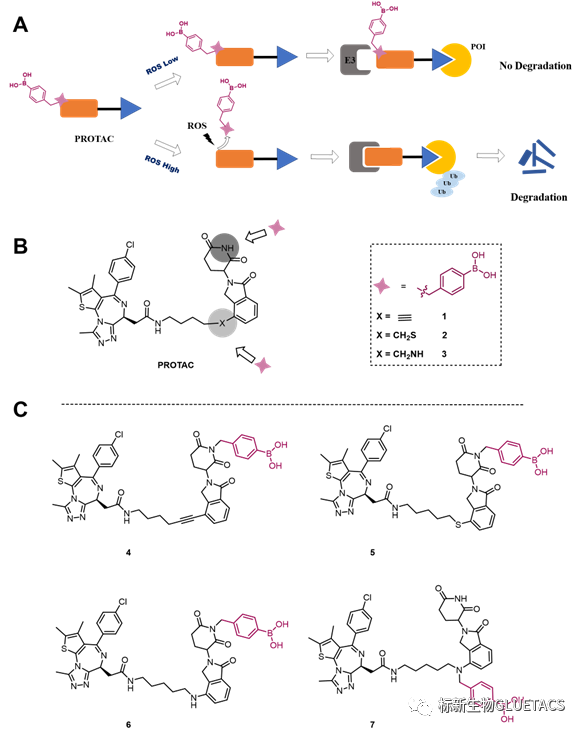
图2 ROS-responsive Pre-PROTAC的机理及设计理念
与上皮样肾胚细胞293T相比,肿瘤细胞T47D的ROS含量远远高于293T细胞。此外,T47D细胞中,Pre-PROTAC(7)可以显著降解BRD3,降解浓度与活性降解剂PROTAC(3)相当。在293T细胞中,只有PROTAC(3)可以降解BRD3,而Pre-PROTAC(7)不降解。这表明Pre-PROTAC(7)是ROS含量依赖的蛋白降解剂。在T47D肿瘤细胞中,Pre-PROTAC(7)和PROTAC(3)对BRD3的降解起效时间也相当,8小时内即可显著降解BRD3。如图3所示。
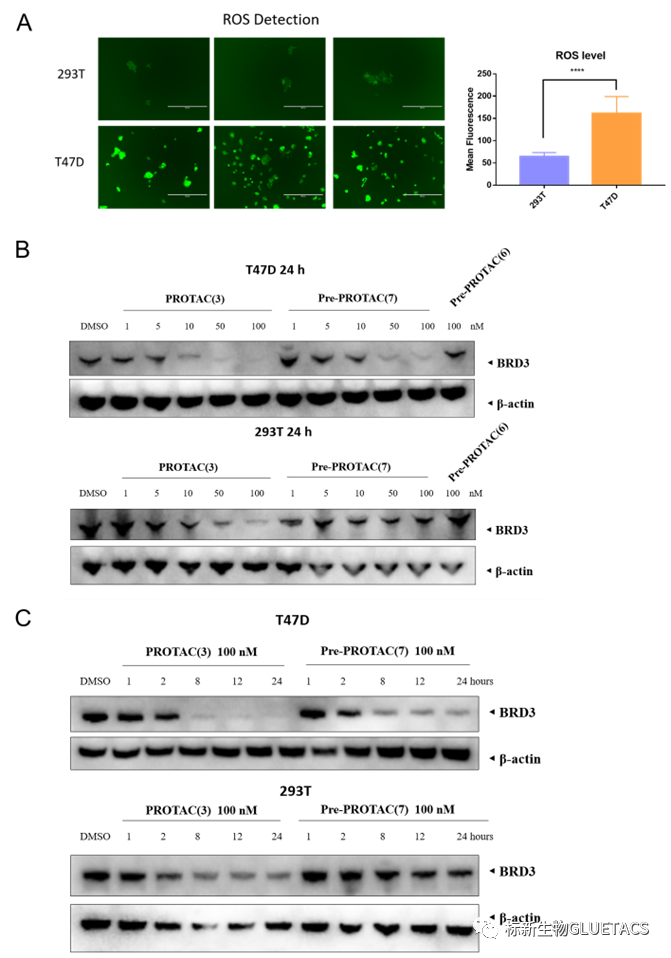
图3 ROS-responsive Pre-PROTAC在肿瘤细胞中特异性降解BRD3
在T47D中使用ROS清除剂NAC预处理,Pre-PROTAC(7)引发的BRD3的降解也会被抑制。经过泛素-蛋白酶体通路抑制剂MLN4924或MG132预处理后,BRD3的降解也会被抑制。这充分验证了Pre-PROTAC(7)以ROS依赖的方式通过泛素-蛋白酶体路径降解致病蛋白的机理。如图4所示。

图4 ROS清除剂NAC或蛋白酶体抑制剂可抑制Pre-PROTAC(7)引起的蛋白降解
利用肿瘤ROS含量高的特点,设计ROS含量依赖的降解剂可以降低在正常组织中蛋白降解剂的活性,只在肿瘤中发挥作用,以提高蛋白降解剂的组织特异性,以期达到“增效减毒”效果。
标新生物研发平台上一系列丰富的技术储备为其进一步实现科研转化及产品临床推进奠定了坚实的理论基础。此次研究成果的发表,充分体现了标新生物研发平台重要的学术价值以及差异化的管线潜力。